فرایند تولید متانول یک فرایند فشار پایین میباشد. متانول با استفاده از گاز طبیعی، گازهای حاصل از فرایندهای پالایشگاهی، گازسنتز، زغال سنگ، کک و یا حتی بیومس تولید میگردد. شکل (1) نشان دهنده شمایی ساده از فرآیند کلی تولید متانول است.
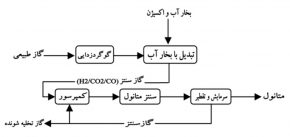
شکل (1): شمایی ساده از فرآیند تولید متانول
به طور صنعتی متانول از ذغال سنگ یا گاز طبیعی سنتز میگردد. فرایند ریفورمینگ در تولید مواد شیمیایی متانول به صورتهای مختلفی انجام میشود ازجمله انواع ریفورمینگ مورد استفاده در این فرآیند عبارتند از:
- استیم ریفرمینگ
- ریفرمینگ فشرده
- اتوترمال ریفرمینگ
- ریفرمینگ ترکیبی
- ریفرمینگ گاز داغ
مراحلی مانند فشرده سازی و سنتز متانول بعد از عملیات ریفرمینگ انجام میگردد. متانول خام در واحد جداسازی از آب، اتانول و سایر ترکیبات جدا میشود. این ناخالصیها در سیستمی که شامل دو ستون تقطیر است جدا میشوند. در ستون اول ناخالصی های سبک مانند اترها، استرها، استن و هم چنین گازهای غیر قابل انحلال حذف میشوند و در ستون دوم نیز آب و الکل های سنگین تر و مواد ارگانیک سنگین مشابه از جریان حذف خواهند شد.
برای خنثی نمودن گازهای اسیدی از هیدروکسید پتاسیم (KOH) در این فرایند استفاده میشود. همچنین جهت تنظیم pH و مقاومت بهتر سیستم در برابر خوردگی از مورفولین (Morpholine) در فرایند تولید متانول استفاده میشود. امروزه به غیر از کشور چین که برای خوراک متانول تولیدی از ذغال سنگ استفاده میکند سایر مناطق جهان برای تولید متانول از گاز طبیعی ارزان قیمت به عنوان خوراک استفاده میگردد.
از نظر اقتصادی، این که انتخاب هرکدام از تکنولوژی گاز سنتز و یا ذغال سنگ به منظور تولید متانول میتواند بهتر باشد، متفاوت است. در چین به دلیل وجود منابع عظیم زغال سنگ، ساخت واحدهایی بر اساس این تکنیک در اولویت قرار دارد. هم چنین در سطح جهان این تمایل وجود دارد که واحدهای فرا ساحل به دلیل دسترسی به مخازن ارزان قیمت تر گاز، استفاده از تاسیسات استخراج نفت برای تولید متانول از گاز طبیعی استفاده شود. برای تهیه و سنتز متانول با گاز طبیعی روشهای متفاوتی وجود دارد این روشها عبارتند از:
- رفرمینگ با بخار آب
- اکسایش جزیی
- اکسایش جزیی کاتالیستی
- فتوشیمیایی
- فتوکاتالیستی
برای تبدیل گاز طبیعی به متانول از دو روش مستقیم و غیر مستقیم استفاده میگردد. در روش مستقیم واکنش سنتز وجود نداشته و متان مستقیما در دما و فشار بالا به متانول تبدیل میگردد که به دلیل شرایط عملیاتی ویژه (دما و فشار بالا) استفاده از این روش در صنعت محدود میباشد.
روش غیر مستقیم در سه مرحله انجام میگردد. در مرحله اول ابتدا متان با آب واکنش داده و منوکسید کربن و هیدروژن حاصل میگردد که این واکنش طبق معادله (1) انجام شده و آن را تولید گاز سنتز مینامند. به دلیل اهمیت این مرحله و این که به شدت گرماگیر میباشد و نیاز به انرژی زیادی دارد حدود 60 درصد از هزینه کل فرایند مربوط به این مرحله میباشد.

در مرحله دوم گاز سنتز تولید شده در مرحله اول به متانول تبدیل میشود:

بعد از تولید متانول در مرحله سوم متانول از سیستم جدا شده و گازهای تبدیل نشده در جریان برگشتی برای تولید مجدد متانول به سیستم برمیگردد.
تولید متانول به روش نوین (گرین متانول)
متانول يکی از محصولات شيميايی پرکاربرد و پایه میباشد که می توان آن را با استفاده از دی اکسيدکربن جمع آوری و ذخیره شده تولید نمود. واحد تولید متانول یکی از واحد های مهم پتروشیمیایی میباشد. در ایران به دلیل وجود ذخایر گازی غنی به عنوان یکی از تولید کنندگان اصلی متانول به شمار میرود.
تاکنون 5 واحد متانول با ظرفیت تولیدی 5 میلیون تن در سال ایجاد شده و حدود 12 واحد با ظرفیت 19 میلیون تن در سال در حال بررسی و راه اندازی می باشد. علت اصلی توجه به تولید متانول با دی اکسید کربن بازیابی شده، تولید متانول از هرگونه منبع دی اکسید کربن میباشد.
اين مزیت باعث شده که برای کاهش دی اکسید کربن به عنوان یک گاز گلخانه ای بتوان از هر منبع از دی اکسید کربن تولیدی استفاده نمود و آن را وارد چرخه بازیابی نمود. در اين چرخه دی اکسید کربن از هر منبعی جمع آوری میگردد و در واکنش با هيدروژن به متانول تبديل شده و مورد بازيابی قرار می گيرد. در این چرخه هیدروژن مورد نیاز به طور کامل مستقل از سوختهای فسیلی و با استفاده از الکترولیز تولید میگردد.
در این چرخه متانول تجدید پذیر میباشد بدین صورت که در دیگر فرایندها با استفاده از متانول ترکیبات نفتی مانند اتيلن، پروپيلن، بنزين و محصولات ديگری که جزء مشتقات نفت و گاز به حساب می آيند تولید میگردد و در ادامه به محض احتراق این محصولات مجدد دی اکسید کربن تولید و به هوا منتشر میگردد که دوباره بازیابی و جمع آوری شده و به چرخه تولید متانول ارسال میگردد. تبدیل دی اکسید کربن به ترکیبات آلی و تهیه سوختها از مفیدترین روش ها برای کاهش دی اکسید کربن میباشد.
فرآیند تولید هیدروژن جهت سنتز متانول
هیدروژن در طبیعت به صورت خالص وجود ندارد اما میتوان آن را توسط چندین روش مختلف از سایر عناصر به دست آورد. فرآیند تولید هیدروژن جهت سنتز متانول خود یکی از موضوعات در خور توجه است و روشهای متنوعی برای تولید آن وجود دارد. به عنوان مثال از جمله روشهای تولید هیدروژن میتوان به روشهای زیر اشاره کرد:
- تولید هیدروژن از منابع فسیلی (تجدید ناپذیر)
- اکسیداسیون جزئی نفت سنگین
- مبدل گاز طبیعی با فرآیند تبدیل گاز توسط بخار
- مبدل گاز طبیعی اکسیداسیون جزئی
- تولید هیدروژن از منابع غیر فسیلی (تجدید پذیر)
- فتوالکتروشیمیایی
- بیولوژیکی
- بیوشیمیایی
- ترموشیمیایی
- ترمولیز، رادیولیز و الکترودیالیز آب
- مواد زیست توده
در کل روشهای تولید هیدروژن یا به صورت بدون کربن بوده یا از طریق سوخت های فسیلی به دست میآیند. از جمله روش های بدون کربن میتوان استفاده از انرژی هستهای، انرژی باد و خورشید را نام برد در روش های بر پایه سوخت های فسیلی گاز سنتز تولید کرده و از این طریق هیدروژن تولید میشود.
به منظور کاهش انتشار CO2 هیدروژن برای تولید متانول بهتر است از یک روش بدون کربن تولید شود. بدین منظور میتوان هیدروژن را از الکترولیز آب با استفاده از یک منبع تجدیدپذیر برق به عنوان یک منبع بدون کربن در نظر گرفته شود. زیست توده، تابش خورشید و باد نیز رایج ترین منابع تجدیدپذیر هستند که برای تامین برق در الکترولیز آب پیشنهاد شده اند، درحالی که باد درحال حاضر یکی از منابع موثر و غنی در میان انرژی های تجدیدپذیر است.
هر چند روشهای متنوعی امروزه به منظور تولید هیدروژن ارائه شده است اما درحال حاضر حدود %98 از کل هیدروژن تولید شده در جهان از سوختهای فسیلی به دست میآید. در جدول (1) از جمله روشهای تولید هیدروژن به همراه منبع انرژی مصرفی و مواد مورد نیاز آورده شده است.
جدول (1): روشهای تولید هیدروژن به همراه منبع انرژی مصرفی و مواد اولیه
| 3 | نام روش | منبع انرژی مصرفی | مواد اولیه |
| 1 | Electrolysis | الکتریکی | آب |
| 2 | Plasma Arc Decomposition | — | سوخت فسیلی |
| 3 | Thermolysis | گرمایی | آب |
| 4 | Thermochemical Processes Water Splitting | — | آب |
| 5 | Thermochemical Processes Biomass Conversion | — | بیومس |
| 6 | Gasification | — | — |
| 7 | Reforming Thermochemical Processes | — | — |
| 8 | PV Electrolysis | فوتونیک | آب |
| 9 | Photocatalysis | — | — |
| 10 | Photoelectrochemical Method | — | — |
| 11 | Dark Fermentation | بیوشیمیایی | بیومس |
| 12 | High Temperature Electrolysis | الکتریکی و گرمایی | آب |
| 13 | Hybrid Thermochemical Cycles | — | — |
| 14 | Coal Gasification | — | — |
| 15 | Fossil Fuel Reforming | — | — |
| 16 | Biophotolysis | فتونیک و بیوشیمیایی | بومس و آب |
| 17 | Photofermentation | — | — |
| 18 | Artificial Photosynthesis | — | — |
| 19 | Photoelectrolysis | الکتریکی و فتونیک | آب |
لازم به ذکر است هیدروژن تولیدی در صنعت به عنوان یک فرآورده شیمیایی به حساب میآید و فروش تجاری هیدروژن کمتر از %10 میزان تولید آن در دنیا میباشد، بدین معنی که %90 هیدروژن تولیدی در محل تولید به مصرف میرسد.
در ادامه به تشریح مختصری در ارتباط با برخی از روشهای تولید هیدروژن پرداخته شده است.
تولید هیدروژن با استفاده از تبدیل گاز طبیعی با بخار آب
تبدیل گاز طبیعی توسط بخار یکی از روشهای متداول تولید هیدروژن میباشد. متان (عنصر اصلی گاز طبیعی) در واکنش تعادلی با بخار شرکت میکند و محصول واکنش به طور عمده هیدروژن و گاز منوکسیدکربن طی واکنش (3) است:

علاوه بر متان سایر هیدروکربنها نیز میتوان در واکنش تبدیل با بخار آب تولید هیدروژن نمایند. از این رو شکل عمومی واکنش تبدیل بخار آب را میتوان به صورت (4) نشان داد:
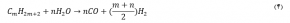
نقش اصلی بخار در واکنشهای تبدیل با بخار منتقل کردن واکنش به سمت تولید محصولات یعنی تولید هیدروژن و کربن مونوکسید است و با توجه به تعادلی بودن واکنش، برای تولید بیشتر هیدروژن و مونوکسید کربن باید واکنش در شرایط دمای بالا و فشار پائین انجام شود.
معمولا این واکنش در فشار ثابت انجام میشود، بنابراین به منظور بالا بردن درجه حرارت به سمت تولید هیدروژن پیش میبرد. برای تأمین چنین حرارت بالایی 900-800 راکتوری که واکنش در آن انجام میشود را در بخش تشعشعی یک کوره قرار میدهند. شکل (2) شمایی ساده از فرآیند تولید هیدروژن با این روش را نشان میدهد.
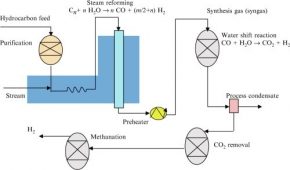
شکل (2): شمایی ساده از فرآیند تولید هیدروژن با استفاده از تبدیل گاز طبیعی با بخار آب
تولید گاز هیدروژن با استفاده از اکسیداسیون جزئی گاز طبیعی
در مواردی که استفاده از گاز طبیعی اقتصادی نباشد از اکسیداسیون جزئی برای تولید هیدروژن استفاده میشود. واکنشهای اکسیداسیون جزیی در این فرآیندی که به صورت واکنشهای ذیل است صورت میگیرد:
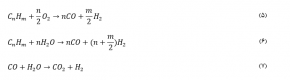
اکسیداسیون جزیی یک واکنش گرمازا بوده و در دمای بالا و در محدوده 1200-1500 بدون وجود کاتالیست انجام میگیرد. مزیت استفاده از این روش بر فرآیندهای کاتالیستی عدم نیاز به حذف ترکیبات گوگردی از خوراک است. همچنین دمای بالا در اکسیداسیون جزیی استفاده از برشهای نفتی سنگین تر که در فرایندهای کاتالیستی قابل مصرف و تبدیل به هیدروژن نبودهاند را در این فرایند امکان پذیر میسازد.
همچنین این فرآیند ممکن است در حضور کاتالیستهای پلاتین و نیکل نیز انجام شود. بازدهی فرآیند اکسیداسیون جزیی نسبت به فرآیند تبدیل با بخار آب، کمتر است و میزان هیدروژن کمتری به ازای هر مولکول متان تولید میگردد. برای تهیه خوارک پیلهای سوختی مبدل اکسیداسیون جزئی مورد استفاده قرار میگیرد.
در این مبدل با تغییر نسبت هوا به سوخت، حرارت واکنش و در نتیجه حرارت راکتور کنترل میشود و نیاز به مبدل دیگری نیست. شکل (3) نشان دهنده شمایی ساده از تولید هیدروژن با استفاده از فرآیند اکسیداسیون جزئی است.
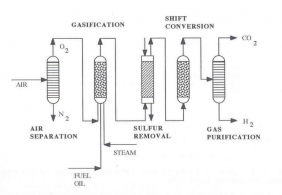
شکل (3): تولید هیدروژن با استفاده از فرآیند اکسیداسیون جزئی
تولید هیدروژن با استفاده از Auto Thermal
در این فرآیند اکسنده که معمولا اکسیژن و یا هوا است به قسمت مشعل راکتور وارد گردیده و سپس از روی سطح کاتالیست در دمای بالا عبور میکند.
واکنشها در این فرایند مخلوطی از واکنشهای گرمازای اکسیداسیون جزیی و گرماگیر بدیل با بخار آب است و در واقع انرژی مورد نیاز واکنش تبدیل با بخار آب توسط واکنش اکسیداسیون جزئی تأمین میگردد. بنابراین میتوان با تغییر نسبت هوا به سوخت دمای واکنش و در نتیجه دمای راکتور را کنترل نمود. شکل کلی واکنشی که در این فرآیند انجام میشود در واکنش (8) ارائه شده است.
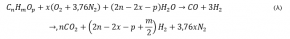
در واکنش فوق زیاد شدن مقدار نسبت هوا به سوخت که با X نشان داده شده است، شدت گرماگیری کاهش مییابد تا این که در یک نسبت خاص، واکنش نه گرماگیر و نه گرمازا است. به همین دلیل است که این نوع مبدل، مبدل را Auto thermal مینامند. مزیت این فرایند نسبت به سیستمهای معمول مصرف بخار آب کم به بخار و نیز تأمین حرارت مورد نیاز به وسیله احتراق بخشی از سوخت است.
تبدیل هیدروژن با استفاده از فرآیند پیرولیز
فرآیند دیگری که به منظور تولید هیدروژن از هیدروکربنها وجود دارد عبارتست از حرارت دادن هیدروکربنها در غیاب هوا که طی این فرآیند، هیدروکربنها شکسته شده و به هیدروژن و کربن تجزیه میگردند. مهمترین مزیت فرآیند شکست حرارتی، تولید هیدروژن با خلوص بالا است.
با افزودن هوا به راکتور داغ، کربن به صورت دی اکسیدکربن از سیستم خارج میشود. در برخی از موارد استفاده از فرایند شکست حرارتی پروپان برای تأمین هیدروژن جهت کاربرد در سیستمهای پیل سوختی پلیمری پیشنهاد شده است.
تولید هیدروژن با استفاده از گازی شدن زغال سنگ
جهت تولید هیدروژن یا گاز غنی از هیدروژن، زغال سنگ با استفاده از اکسیژن خالص در درجه حرارت و فشارهای بالا به صورت گازی شکل در آمده و هیدروژن طبق واکنشهای ذیل تولید میگردد:

شکل (4) نیز نشان دهنده شمایی ساده از فرآیند تولید گاز هیدروژن به وسیله فرآیند گازی شدن ذغال سنگ است.
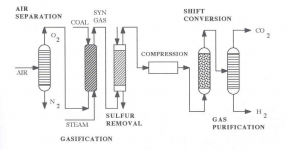
شکل (4): شمایی ساده از فرآیند تولید گاز هیدروژن به وسیله فرآیند گازی شدن ذغال سنگ
تولید هیدروژن با استفاده از فرآیند بخار آهن
یکی از قدیمی ترین فرآیندها به منظور تولید هیدروژن استفاده از فرآیند بخار آهن است. این فرآیند بر پایه زغال سنگ بنا شده و گاز حاصل از زغال سنگ به منظور احیاء اکسید آهن و تبدیل آن به آهن کاربرد دارد. در این فرآیند در مرحله اول زغال سنگ تحت تأثیر بخار و هوا برای تولید گازهای احیا کننده هیدروژن و منوکسیدکربن طی واکنش زیر به کار برده میشود:

در مرحله دوم این گازها با اکسیدهای آهن واکنش داده و اکسیدهای آهن احیا شده را مطابق واکنشهای زیر تولید میکنند:

در سومین مرحله واکنش اجزاء احیاء شده در حضور آب اکسید شده و آهن تولید شده وارد راکتور بخار – آهن میگردد و در پایان و گاز غنی از هیدروژن تولید میگردد. شکل (5) نیز نشان دهنده شمایی ساده از فرآیند تولید هیدروژن با استفاده از فرآیند بخار آهن است.
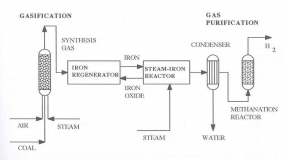
شکل (5): شمایی ساده از فرآیند تولید هیدروژن با استفاده از فرآیند بخار آهن
فرایند تولید متانول از دی اکسید کربن
روش های مختلفی برای تولید متانول از دی اکسید کربن وجود دارد که در ادامه این بخش به بررسی برخی از اين روشها پرداخته شده است. به طور کلی روشهای تولید متانول از دی اکسید کربن عبارتند از:
- روش مستقیم هیدروژناسیون دی اکسیدکربن
- روش غیر مستقیم هیدروژناسیون دی اکسیدکربن
- روش فوتو الكتروشیمیایی
- روش زیست الكتروشیمیایی
- روش گرما شیمیایی
- روش الكتروشیمیایی
- تبدیل فوتو کاتالیستی
در روش تولید متانول با استفاده از دی اکسید کربن، دی اکسید کربن و هیدروژن از روشهای غیر از سوختهای فسیلی به دست میآیند، به همین دلیل متانول تولیدی متانول سبز و تجدید پذیر نامیده میشود. در حال حاضر روش تولید هیدروژن روش الکتروليز آب بوده که طی آن هيدروژن و اکسيژن توليد میشود. شکل (6) نشان دهنده شمایی کلی از فرآیند تولید متانول با استفاده از هیدروژن است.
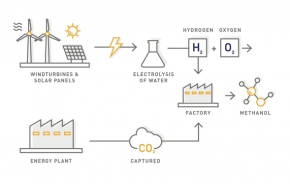
شکل (6): شمایی کلی از فرآیند تولید متانول با استفاده از هیدروژن
روش مستقیم هیدروژناسیون دی اکسید کربن
در این روش، دی اکسیدکربن و هیدروژن به طور مستقیم به متانول تبدیل میشوند. در این فرآیند مطابق با واکنشهای زیر، نسبت دی اکسید کربن به هیدروژن 1 به 3 میباشد. این مقدار به طور مستقیم وارد مخزن تولید متانول میگردد. در این فرایند مقدار زیادی منوکسیدکربن تولید میگردد بنابراین انتخاب پذیری واکنش متانول نسبت به منوکسید کربن بیشتر میباشد. به غیر از منوکسید کربن ترکیباتی همچون دی متيل اتر و متان به عنوان محصولات جانبی تولید میگردد. واکنشهای انجام گرفته در اين روش عبارتند از:

ابتدا جریان خروجی سرد سپس وارد برج جداکننده میگردد. در این فرایند مواد اولیه ای مانند دی اکسید کربن و آب وجود دارند که وارد واکنش نشدهاند. متانول آنها جدا شده و آب و دی اکسید کربن مجدد به برج تولید متانول فرستاده میگردد. هیدروژن نیز با استفاده از فرايند جذب سطحي از گاز اضافی جدا شده و مابقی آن نیز صرف احتراق میگردد.
روش دو مرحله ای تولید متانول از دی اکسید کربن (RWGS)
در روش دو مرحلهای یا غیر مستقیم تبدیل دیاکسیدکربن به متانول از روش واکنش انتقال گاز معکوس استفاده میگردد. اولین مرحله، در واکنش هیدروژناسیون دی اکسید کربن از طریق واکنش[1](RWGS) گاز سنتز تولید میشود و سپس در مرحله دوم گاز سنتز تولید شده به یک راکتور به عنوان ماده اولیه برای تولید متانول انتقال مییابد. سنتز متانول توسط فرآیند CAMERE شامل یک راکتور RWGS و یک راکتور سنتز متانول میباشد. مواد اولیه مورد نیاز در این روش دی اکسید کربن و هیدروژن میباشد.
در مرحله اول واکنش تولید گاز سنتز از دی اکسید کربن یک واکنش تعادلی گرماگیر بوده و در دمای بالا انجام میگیرد. بنابراین از کاتالیستهایی مانند ZnO/Al2O3 استفاده میشود و در دماهای بیشتر از 650 درجه سانتی گراد واکنش میتواند به شرایط تعادلی برسد.
در این روش نیز مانند روش تک مرحله ای جریان خروجی از راکتور اول سرد گردیده و وارد برج جداکننده میشود در برج جداکننده آب آن جدا شده و باقی مانده که شامل منوکسید کربن، دی اکسید کربن و هیدروژن میباشد با مقداری هیدروژن اضافی وارد برج دوم که سنتز متانول در آن صورت میگیرد ارسال میگردد. در راکتور دوم نیز واکنش در دمای بالا صورت میپذیرد.
ترکیباتی همچون دي متيل اتر و متان نيز به عنوان محصول جانبی همراه با متانول تولید میگردند. بعد از مرحله دوم جریان خروجی تا دمای 30 درجه سانتیگراد سرد و با ارسال آن به برج جداکننده فاز گاز و مایع آن جدا میگردد.
فاز گاز جدا شده مجدد به راکتور دوم برگردانده و اجزای غیرفعال برای احتراق از حلقه تولید متانول جدا میشوند. قبل از ارسال آنها برای احتراق مشابه مرحله قبل هیدروژن آن جذب میگردد. فاز مايع جدا شده، نیز به برج تقطیر برای جداسازی متانول آن ارسال میگردد. متانول حاصل از تقطير بسيار خالص است و غلظت آن چیزی در حدود 8/99 درصد میباشد. شکل (7) نشان دهنده شمایی کلی از فرآیند تولید متانول با استفاده از فرآیند RWGS است.
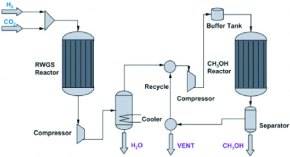
شکل (7): شمایی کلی از فرآیند تولید متانول با استفاده از فرآیند RWGS
روش فوتو الكتروشیمیایی
افزایش گازهای گلخانهای و همچنین افزایش دی اکسید کربن موجود در اتمسفر باعث توجه بیشتر برای تبدیل این گاز به سوخت شده است. در تولید موادی همچون متانول و متان از احیای فوتوالکتروشيميايی دی اكسيد کربن استفاده میشود. در اين روش، از یک کاتالیست نیم رسانا به همراه نور استفاده میگردد. این کاتالیست روی الکترودها قرار گرفته و با جذب انرژی نوری حفره و جفت الکترون تولید میکند. با پیشرفت واکنش الکترون ها و پروتونهای تولید شده منجر به تبدیل دی اکسید کربن میگردد. واکنش زیر نشان دهنده این فرآیند است.

فرایندهای مهم در این مرحله عبارتند از:
- مرحله اول تابش نور به کاتالیست که منجر به تولید جفت الکترون- حفره میگردد.
- مرحله دوم شروع واكنش ماده جذب شده
- مرحله سوم شروع واكنش مواد حد واسط
- مرحله آخر تشکیل محصول و آزاد شدن آن از سطح واکنش
روش زیست الكتروشیمیایی
در روش زیست الكتروشیمیایی از میکرو ارگانیسمها به عنوان کاتالیزور در واکنشهای اکسایش و کاهش استفاده میشوند. میکرو ارگانیسمها میتوانند به عنوان پذیرنده الکترون عمل کنند.
خاصیت تکثیری میکروارگانیسم ها، عملکرد مناسب میکروارگانیسمها در pH خنثی و دمای پایین و همچنین ارزان بودن الکترودهای کربنی در این روش منجر به استفاده بیشتر از روش زیست الكتروشیمیایی برای تبدیل دی اکسید کربن به متانول شده است. از این روش همچنین برای توليد هيدروژن، هيدروژن پروكسيد و اتانول استفاده میگردد. عواملی همچون نوع میکروارگانیسم، واکنش آنها و تعداد میکرو ارگانیسمها در سطح الکترود بر کیفیت تبدیل دی اکسید کربن موثر میباشند.
روش گرما شیمیایی
در روش گرما شیمیایی انرژی گرمایی به انرژی شیمیایی تبدیل میشود. برای تبدیل دی اکسید کربن به گاز سنتز به روش گرماشیمیایی برای انتقال گرما (دمای 1100 درجه سانتی گراد) از لوله های مقاوم در مقابل گرما استفاده میشود. برای تولید سوخت در این روش ابتدا اکسیژن با کاهش گرمایی اکسیدهای فلزی تولید و سپس با اکسایش مجدد اکسیدهای فلزی کاهش یافته توسط دی اکسید کربن یا آب منوکسید کربن و هیدروژن تولید میگردد. در مرحله اول که اکسیژن تولید میشود سرعت واکنش بالا بوده اما در مرحله بعد واکنش به صورت کند انجام میگردد.
با افزایش دما در مسیرهای تولید گرما در تولید گاز سنتز توسط آب و دی اکسید کربن، انتقال گرما بهتر صورت گرفته و راندمان نهایی را بهبود میبخشد. گاز سنتز تولیدی به عنوان مواد اولیه برای تهیه سوختهای مایع استفاده میگردد. واكنش های زير، مسير فرآيند تبديل گرماشيميايی دی اكسيد کربن را در حضور اكسيد های فلزي نشان میدهند:
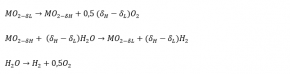
اگر در واكنش آخر به جاي H2O ، CO2 قرار گيرد واکنش زیر بدست می آید:

در اين واكنش ها، MO اكسيد فلزي و δL و δH نسبتهاي غيراستوكيومتری اكسيژن در دماهاي پايين و بالا را نشان ميدهند.
روش الكتروشیمیایی
یکی از روشهای تبدیل دی اکسید کربن به الکل ها روش الکتروشیمیایی میباشد. در این روش از کاهش الکتروشیمیایی دی اکسید کربن به متانول استفاده میشود. روش الکتروشیمیایی روشی است که برای ذخیره انرژی الکتریکی بدون این که میزان دی اکسیدکربن افزایش یابد، استفاده میشود. واکنش الکتروشیمیایی بین الکترود و الکترولیت انجام میشود.
در آند آب اکسید شده و در کاتد الکترون آزاد میگردد که این الکترودها منجر به کاهش دی اکسید کربن به متانول میشود. از این روش برای تولید هیدروکربن توسط کاهش دی اکسید کربن نیز استفاده میگردد. این روش به عنوان یک روش کار آمد برای تبدیل دی اکسید کربن در شرایط ملایم شناخته شده است. واکنش اکسایش و کاهش در این روش به صورت زیر میباشد.
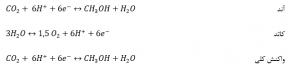
شکل (8) نشان دهنده شمایی کلی از فرآیند تولید متانول با استفاده از فرآیند الكتروشیمیایی است.
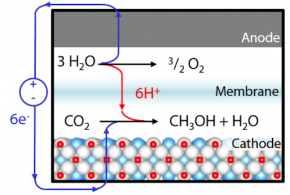
شکل (8): شمایی کلی از فرآیند تولید متانول با استفاده از فرآیند الكتروشیمیایی
تبدیل فوتوکاتالیستی
یکی از روش های تبدیل دی اکسید کربن به سوخت و مواد با ارزش تبدیل فتوکاتالیستی دی اکسید کربن میباشد. در این روش از نور خورشید و یک نیم رسانا استفاده میشود. با استفاده از نانو فتوکاتالیست ها می توان از انتشار دی اکسید کربن جلوگیری و منجر به تولید محصولات مفید در دمای محیط نمود. تیتانیوم دیاکسید، اکسید روی و سولفیدکادمیم از جمله نیم رساناهای کاتالیستی هستند که برای تبدیل فتوکاتالیستی دی اکسید کربن به متانول و فرمالدهید استفاده میشود.
استفاده از روش های تبديل فوتوالکتروشيميايی و فوتوكاتاليستی به دلیل استفاده از نور خورشید به عنوان انرژی فرایند و دمای عملیاتی پایین از اهمیت بالایی برخوردار میباشند زیرا هیدروژن دار کردن دی اکسیدکربن در دما و فشار بالا صورت میگیرد و نیازمند انرژی بالا میباشد. اولین بار در سال 1979 هوندا و همکارانش از طریق کاهش فتوکاتالیستی دی اکسید کربن را به متانول تبدیل نمودند. در این روش از ذرات نیم رسانای اکسیدهای فلزی و غیرفلزی در آب استفاده نمودند.
از معایب روش فتوکاتالیستی برخلاف پتانسیل بالا میتوان به متناسب نبودن توانایی جذب نیم رسانا و جذب طیف نوری، عدم توانایی در جداسازی حاملین بار، کم شدن حلالیت دی اکسید کربن در آب و واکنش های رقابتی احیای مولکول آب اشاره نمود. این روش شامل فرایندهای زیر میباشد:
- توليد جفت الکترون و حفره ها بعد از جذب فوتون های با انرژی مناسب
- جداسازی حاملین بار و انتقال آن ها
- واکنش های شیمیایی بین گونه های سطحی و حاملین بار
واکنش هایی بعد از جذب فوتونها برسطح کاتالیست ممکن است صورت گیرد که توجه به این واكنش ها مهم میباشد. بر اثر برانگیخته شدن نوار شکاف، الکترونهای نوار هدایت و حفره های نوار والانس تشکیل میشود كه، به ترتيب به عنوان جايگاههايي براي اكسايش و كاهش نوري عمل ميكنند. اكسايش نوری بر اثر تابش نور به سطح كاتاليست نيم رسانا باعث تشکيل راديکال هاي هيدروكسيل و يون هاي H+ در حضور حفره هاي نوار والانس میشود كه در ادامه، راديکال های هيدروكسيل به توليد اكسيژن میانجامد و يون هاي H+ را نيز به كمک الکترون های نوار رسانش هيدروژن توليد میكنند.
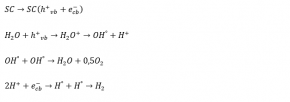
از نظر ترمودینامیکی، دی اكسيد كربن یک مولکول پایدار میباشد که فرایندهای اکسایش و کاهش آن به دشواری صورت می پذیرد. روش تولید متانول با فرایند فتوکاتالیستی دی اکسید کربن روشی پیچیده میباشد. براساس تحقیقات انجام شده مشخص گردید در فرایند فتوکاتالیستی دی اکسید کربن انتقال چندگانه الکترون صورت میگیرد. در ادامه واكنش های ممکن در احيای فتوکاتالیستی دی اكسيد كربن در محيط آبی را نشان داده است:

معادلات فوق که فرايند هاي چند گانه الکتروني هستند معادلات مطلوبی بوده و برای انتقال الکترون به انرژی زیادی مورد نیاز نمیباشد. پتانسيل نوار رسانش كاتاليست هاي TiO2، NiO و ZnO مورد استفاده براي اين واكنشها در pH برابر 7 برابر با 29/0- ، 5/0- و 31/0- است. در مقایسه با پتانسیل استاندارد واکنش ها امکان تولید محصولات مطلوب به اثبات میرسد.
TiO2 يکي از فوتوكاتاليست های مهم براي كاهش دي اكسيد كربن شناخته میشود. با اين حال، اين فوتوكاتاليست نمیتواند نور مرئی را در طيف الکترومغناطيسی جذب كند و تنها میتواند 4 درصد از نور خورشيد دريافتی را مصرف كند كه باعث كاهش بازده فوتوكاتاليستی آن میشود.
شکل (9) نشان دهنده شمایی کلی از فرآیند تولید متانول با استفاده از فرآیند فوتو کاتالیستی است.
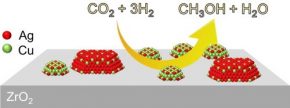
شکل (9): شمایی کلی از فرآیند تولید متانول با استفاده از فرآیند فوتو کاتالیستی