نیترات آمونیوم، با فرمول شیمیایی NH4NO3، نمکی از آمونیاک و اسید نیتریک است که حاوی حدود ۵/۳۳ درصد نیتروژن است. رنگ ماده شیمیایی نیترات آمونیوم از سفید تا خاکستری متمایل به قهوهای و ماده ای بدون بو است و دمای ذوب آن ۱۶۹ درجه سانتیگراد میباشد و در دمای ۲۱۰ درجه سانتیگراد تجزیه میشود.
نیترات آمونیوم هم به شکل مایع و هم به صورت کریستال های جامد موجود است. نیترات آمونیوم یک اکسید کننده قوی است و در صورت تماس با سایر مواد ممکن است باعث آتش سوزی یا انفجار شود. شکل (1) نشان دهنده واکنش شیمیایی بین آمونیاک و نیتریک اسید جهت تولید آمونیوم نیترات است.
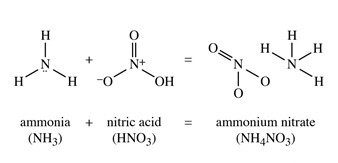
شکل (1): واکنش شیمیایی بین آمونیاک و نیتریک اسید جهت تولید آمونیوم نیترات
با ترکیب نیتروژن موجود در هوا با هیدروژن به دست آمده توسط اصلاح بخار از زغال سنگ یا گاز طبیعی، آمونیاک به یک ماده شیمیایی عظیم تبدیل شد. آمونیاک سپس با ترکیب آن با هوا روی یک کاتالیزور پلاتین داغ و در اصل سوزاندن آن میتواند اکسیده شود و به اسید نیتریک تبدیل شود. به این ترتیب نیترات آمونیوم با فرمول شیمیایی NH4NO3 تولید میگردد.
آمونیاک گرم و اسید نیتریک در یک واکنش خنثی کننده ترکیب می شوند. پس از آب زدایی، نمک مذاب در یک برج اسپری کننده فرو می رود که قطرات در حال سقوط به عنوان توده هایی به اندازه قرص با عنوان قرص های استوانهای شکل نامیده میشوند.
چگالی قرص های تولیدی نیز قابل کنترل است. ماده متراکم تر برای استفاده به عنوان کود مورد استفاده قرار گرفته و ماده سبک تر و متخلخل تر وارد صنعت مواد منفجره می شود. آمونیوم نیترات یک جاذب بسیار قوی رطوبت است، از همین رو در هنگام تولید یک پوشش ضد رطوبت روی آن قرار می دهند. شکل (2) نشان دهنده شمایی ساده از فرآیند تولید آمونیوم نیترات است.
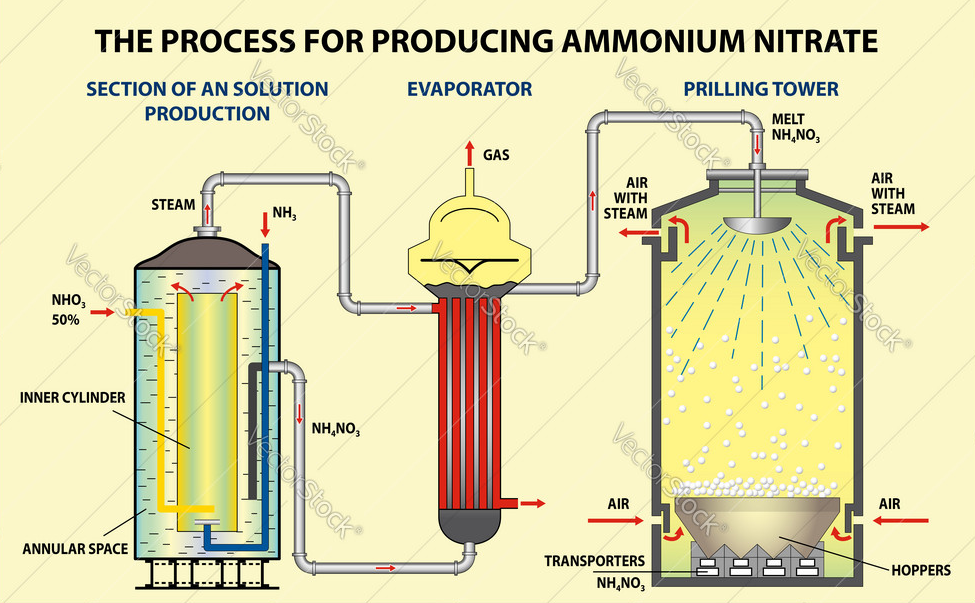
شکل (2): شمایی ساده از فرآیند تولید آمونیوم نیترات
عوامل مختلفی وجود دارد که منجر به تحریک و حتی انفجار آمونیوم نیترات میشود، از جمله این عوامل میتوان به موارد زیر اشاره کرد:
- قرار گرفتن در معرض آلایندهها از جمله کلریدها و فلزاتی مانند کروم، مس، کبالت و نیکل
- قرارگیری در محیطهای اسیدی (کاهش pH)
- در صورت تماس با موادی نظیر روغن، سوخت و کاغذ
مهم ترین کاربرد آمونیوم نیترات استفاده از آن در صنایع کشاورزی است. استفاده از این کود برای محصولات مرتع و علفزار مخصوصا در کشورهای اروپایی، بسیار رایج است به طوری که سالیانه حدود 37 میلیون تن از این ماده در جهان تولید و استفاده می شود. از آنجایی که ریشه گیاهان توانایی جذب مستقیم نیتروژن از طریق خاک را ندارند، نیترات یک منبع عالی برای تغذیه گیاهان است.
کود آمونیوم نیترات از قدیمی ترین کود نیتراته دنیاست که به صورت انبوه تولید شده است. فرم گرانوله این ماده به دلیل سهولت در حمل و نقل و کار با آن، همواره مورد ترجیح کشاورزان بوده است. از دیگر کاربردهای این ماده می توان به استفاده در تولید رنگ، آفت کش، مواد آتش بازی و اکسید کننده ها اشاره کرد.